抗生素被用于治疗危及生命的感染已有近百年,随着日益增加的耐药性细菌的出现,传统疗法对耐药细菌感染已不再有效,抗生素耐药性危机已成为亟待解决的全球健康问题,迫切需要新的下一代抗菌药物(以核酸和肽为基础)的发现方法。
抗菌肽(AMP)存在于所有生命领域,能够导致细胞裂解从而完全杀死或抑制微生物生长。与传统的广谱抗生素相比,AMP 更具针对性,且其耐药性演变速度很低,有望成为一种潜在的治疗方法。
近日,复旦大学类脑智能科学与技术研究院(下文简称“类脑研究院”)青年研究员路易斯·佩德罗·科埃略(Luis Pedro Coelho)、名誉教授皮尔·伯克(Peer Bork)、特聘教授赵兴明团队与来自美国与德国的科学家将人工智能与生物医学交叉融合,从全球微生物组中预测近100万种新型抗菌肽。相关成果以《利用机器学习发现全球微生物组中的抗菌肽》(“Discovery of antimicrobial peptides in the global microbiome with machine learning”)为题,在《细胞》(Cell)主刊上发表。
证明人工智能方法从全球微生物组中识别功能性 AMP 的潜力,为未来抗菌药物的研发迈出重要一步
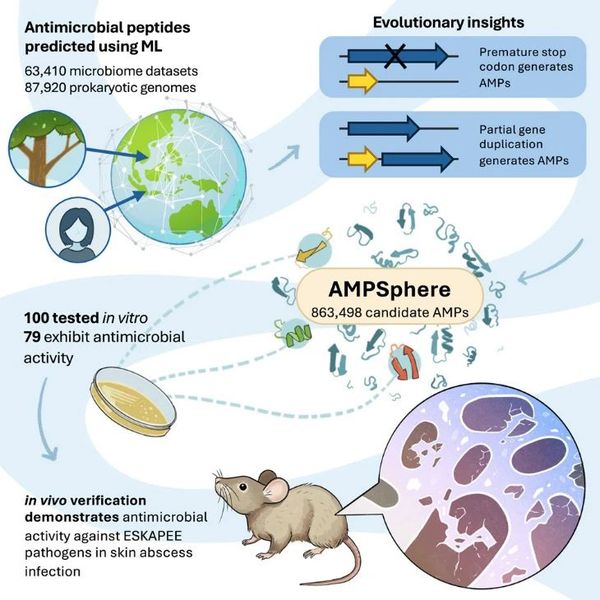
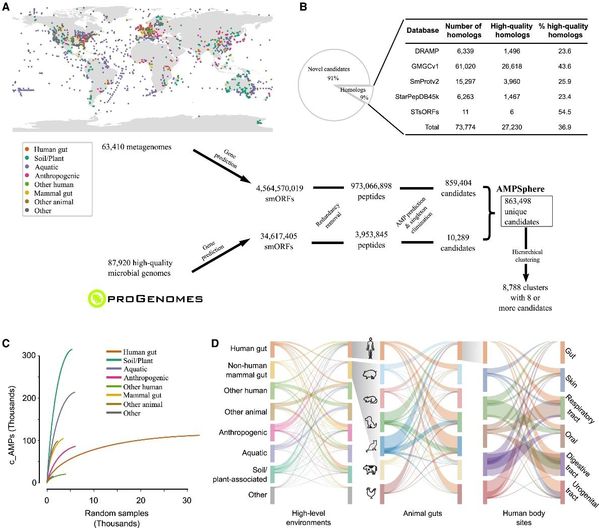
在研究中,团队提出了一种针对微生物多肽识别的机器学习算法,可大大降低抗菌肽(AMP)识别的假阳性率。基于该机器学习算法,研究团队从来自环境和宿主相关栖息地的全球63,410个宏基因组和87,920个高质量细菌与古菌基因组预测得到了近100万种新型非冗余抗菌肽,并建立了AMP综合数据资源(AMPSphere)。
研究发现, AMP 的产生特定于栖息地,且其功效表现出菌株特异性。研究团队测试了 100 种合成的AMP对 11 种临床相关致病菌株和人类肠道共生菌的作用,共有 79 种 AMP表现出针对病原体和/或共生菌的抗菌活性,其中63 种 AMP成功抑制了被认为是公共卫生问题的ESKAPEE病原体的生长。此外,研究团队在小鼠感染模型中发现一些AMP具有抗感染功效,相当于临床前小鼠模型中的多粘菌素B(一种商业临床抗生素,同样是AMP)。
该研究证明了人工智能方法从全球微生物组中识别功能性 AMP 的潜力,研究团队提出的该AMPSphere数据库为微生物领域研究提供了宝贵资源,这些研究发现对于理解抗菌肽的起源和作用机制具有重要意义,为未来抗菌药物的研发迈出了重要一步,为人类健康研究提供了重要贡献。
深耕人工智能与生物医学交叉领域,团队在AI for Science前沿持续探索
近年来,人工智能技术蓬勃发展,已广泛地应用于生物学、神经科学、医学等领域,在蛋白质结构预测、生物基础大模型建立、生物医学图像识别等方面取得了新突破。
复旦大学类脑研究院生物医学人工智能(BioMed AI)团队长期聚焦于人工智能与生物医学交叉研究,团队负责人为复旦大学特聘教授、上海市生物信息学学会理事长、类脑智能科学与技术研究院副院长、计算神经科学与类脑智能教育部重点实验室副主任赵兴明。
此前,在生物医学大数据方面,团队已构建了首个全球微生物基因目录,成果刊发于《自然》主刊,构建了中国人肠道病毒组目录,在国际率先提出了人体真菌肠型的概念并揭示了人类四种真菌“肠型”结构等。与此同时,团队还针对生物医学大数据开发了一系列人工智能算法与工具,如宏基因组组装错误识别与矫正算法metaMIC、基于sMRI的多模态PET指标预测方法等,并成功应用于微生物组学、基因组学、影像组学等不同场景。
本次研究成果为团队将人工智能算法应用于微生物组学的里程碑式进展。据赵兴明介绍,未来,团队将继续聚焦人工智能与生物医学大数据交叉领域的研究,“比如基于中国人肠道病毒组目录开发人工智能算法与工具,进行相关微生物大模型的训练”,在AI for Science的前沿持续探索。
类脑研究院博士后Célio Dias Santos-Júnior与美国宾夕法尼亚大学Marcelo D.T. Torres为共同第一作者,类脑研究院青年研究员Luis pedro Ceolho与美国宾夕法尼亚大学的Cesar de la Fuente-Nunez 为共同通讯作者。
论文链接:https://doi.org/10.1016/j.cell.2024.05.013





