时至今日,癌症仍是人类健康的“头号杀手”,如何实施精准有效的治疗,特别是减轻患者痛苦、延长患者生命,已成为全人类共同关注的重大课题。免疫治疗是癌症治疗的新希望,近日,复旦大学附属中山医院樊嘉院士、高强教授团队在《科学》(Science)和《细胞》(Cell)杂志上分别发表两项重要研究成果,深入剖析了肿瘤免疫微环境的复杂性和功能多样性,突破了既往“以T细胞为核心的免疫治疗”研究模式,为肿瘤免疫治疗的临床和转化研究开辟了新的方向。

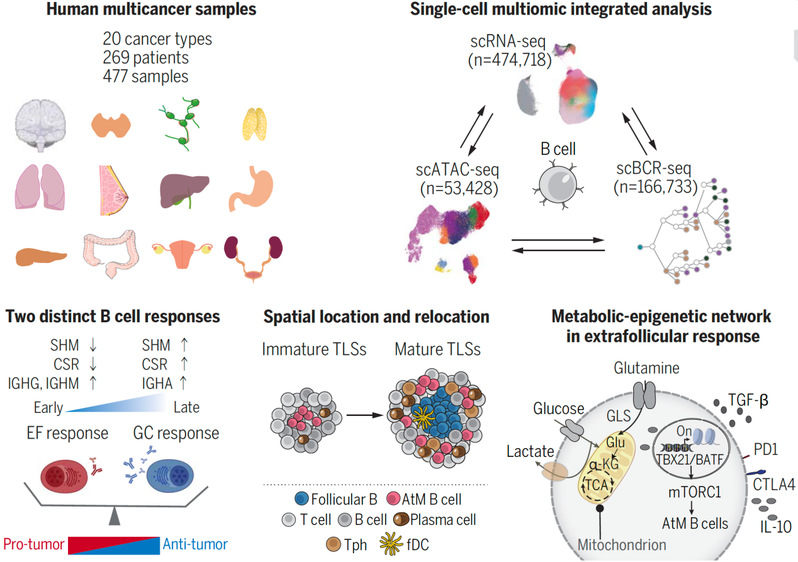
5月3日,复旦大学附属中山医院樊嘉院士、高强教授团队,联合中国科学院上海免疫与感染研究所与浙江大学基础医学院等合作单位,在《科学》(Science)杂志在线发表了题为《人类癌症中肿瘤浸润 B 细胞蓝图》(A blueprint for tumor-infiltrating B cells across human cancers)的论文,系统性揭示了肿瘤微环境B细胞的表型功能异质性、动态分化以及表观调控机制。研究团队分析了肝癌、胆管癌、胆囊癌等多个癌种的临床样本数据发现,B细胞可以分为15个不同功能的亚群。其中,一类叫做DUSP4+非典型记忆B细胞的亚群引起了研究团队的注意。这类细胞通过滤泡外应答途径分化为浆细胞,能够分泌识别自身抗原的抗体,并抑制T细胞的功能,导致肿瘤微环境处于免疫抑制状态,不利于患者的预后和抗癌免疫治疗。这一发现为未来精准调控B细胞、鉴定新的免疫治疗靶点以及开发新的免疫联合治疗方案提供了重要线索。

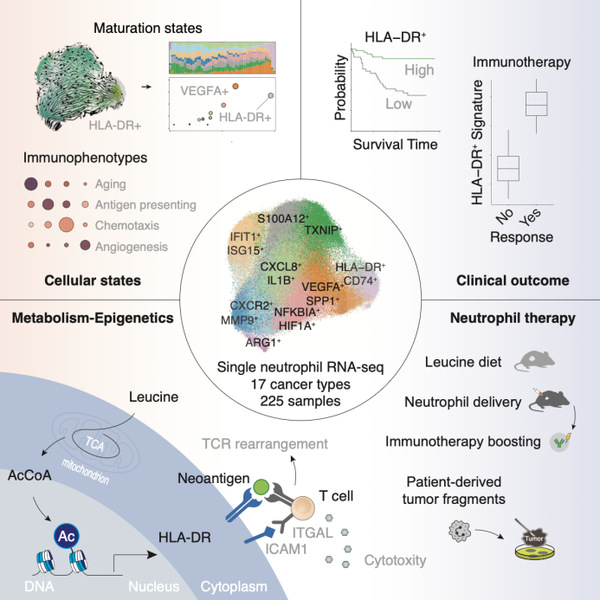
此外,该团队今年2月在《细胞》(Cell)杂志上发表的《中性粒细胞分析阐明抗肿瘤抗原呈递功效》(Neutrophil profiling illuminates anti-tumor antigen-presenting potency)论文中,进一步系统性揭示了中性粒细胞的抗肿瘤功能,探索了利用中性粒细胞的抗原提呈特征来增敏肿瘤免疫治疗的价值和临床意义。研究者同样利用来自肝癌、胆管癌、胆囊癌等多个癌种患者的样本来源的数据,发现一种特殊的中性粒细胞亚群(HLA-DR+CD74+),与患者的临床预后正相关,并能增强T细胞的抗原特异反应且促进形成有利于免疫治疗的热肿瘤微环境。研究团队还发现,饮食中富含的亮氨酸对中性粒细胞的抗原提呈功能有促进作用;富含亮氨酸的饮食或输注HLA-DR+CD74+亚群的中性粒细胞都能够增强PD-1单抗的肿瘤免疫治疗疗效。这提示我们未来可以通过饮食干预等方式来增强患者自身的抗肿瘤免疫力,提高免疫治疗疗效。这项研究为利用中性粒细胞抗原提呈来增敏免疫治疗提供了新的思路,有望推动肿瘤免疫治疗的进一步发展。
当前,肿瘤治疗已进入多学科联合诊疗的“精准医疗”时代,以“PD-1/PD-L1单抗”为代表的免疫治疗作为一种新兴的肿瘤治疗方法已被广泛使用。免疫治疗是依靠患者自身免疫机能识别并杀灭癌细胞,不仅能提高患者的生存,而且避免了传统化疗、放疗的副作用,改善了患者的生活质量。然而,由于个体的差异性和治疗的局限性,免疫治疗并非只有PD-1/PD-L1一条路,需要个体化的新策略和联合治疗方案。
中山医院肝肿瘤外科高强教授指出,B细胞是适应性免疫的关键组成部分,在体液免疫应答和抗体产生方面发挥着至关重要的作用,但由于相关研究不足,其在临床应用上的进一步拓展受到了限制。与此同时,中性粒细胞作为人体天然免疫的第一道防线,广泛参与人体免疫的各个重要环节。但鉴于其半衰期短且细胞脆弱,目前鲜有相关大规模系统研究,这使得中性粒细胞成为肿瘤免疫治疗中的争议焦点。此次研究的重要发现为不仅为肿瘤免疫治疗提供了新的理论支撑,更为提高免疫治疗的精准度和有效性、开发更有效的治疗方法提供了关键线索。
原文链接:
《科学》(Science)https://doi.org/10.1126/science.adj4857





