髓系来源抑制细胞(MDSC)在肿瘤免疫微环境中发挥关键作用,但由于缺乏特异性靶点,针对其的靶向药物开发面临挑战。LILRB4是一种含有ITIM结构域的免疫检查点受体,与MDSC介导的肿瘤免疫抑制有关。尽管针对LILRB4的药物在临床前和临床研究中有所进展,但治疗效果并不理想。目前尚不清楚与肿瘤微环境中的MDSC相关的LILRB4功能性配体,这阻碍了阻断性抗体的开发和伴随诊断。
2024年1月16日,复旦大学生物医学研究院许杰课题组在Cell Reports Medicine杂志上发表了题为“Discovery of Galectin-8 as an LILRB4 ligand driving M-MDSCs defines a class of antibodies to fight solid tumors”的文章,该研究首次报道了Galectin-8作为LILRB4的肿瘤相关功能性配体,通过下游的STAT3和NF-κB通路来诱导M-MDSC,从而促进免疫抑制和肿瘤的生长,并研发了具有阻断功能的治疗抗体,证明了阻断Galectin-8与LILRB4的抗体能够减缓多种高表达Galectin-8的肿瘤在小鼠体内的生长,具有潜在治疗和转化价值。

研究人员发现Galectin-8具有独特的表达模式,并对肿瘤预后和免疫浸润因子产生影响。Galectin-8与MDSC具有相关性,进一步的研究显示Galectin-8与LILRB4以高亲和力结合,调控胞内的SHP-1-STAT3/NF-κB通路。Galectin-8能够诱导M-MDSC的增加并抑制T细胞增殖。利用基因敲除小鼠模型,研究人员证明了LILRB4 的存在和Galectin-8的过表达功能促进小鼠M-MDSC的增加和肿瘤生长。
通过分别开发了抗LILRB4抗体和抗Galectin-8抗体,研究者证明了双向阻断均能够抑制Galectin-8和LILRB4作用带来的效果,并且研究者对抗体的表位进行了分析,特别对于阻断性抗体与LILRB4的结合表位进行了明确定位(下图B-C)。随后,利用人源化小鼠肿瘤模型,研究者证明抗体抑制表达Galectin-8肿瘤的生长(下图K-L)。

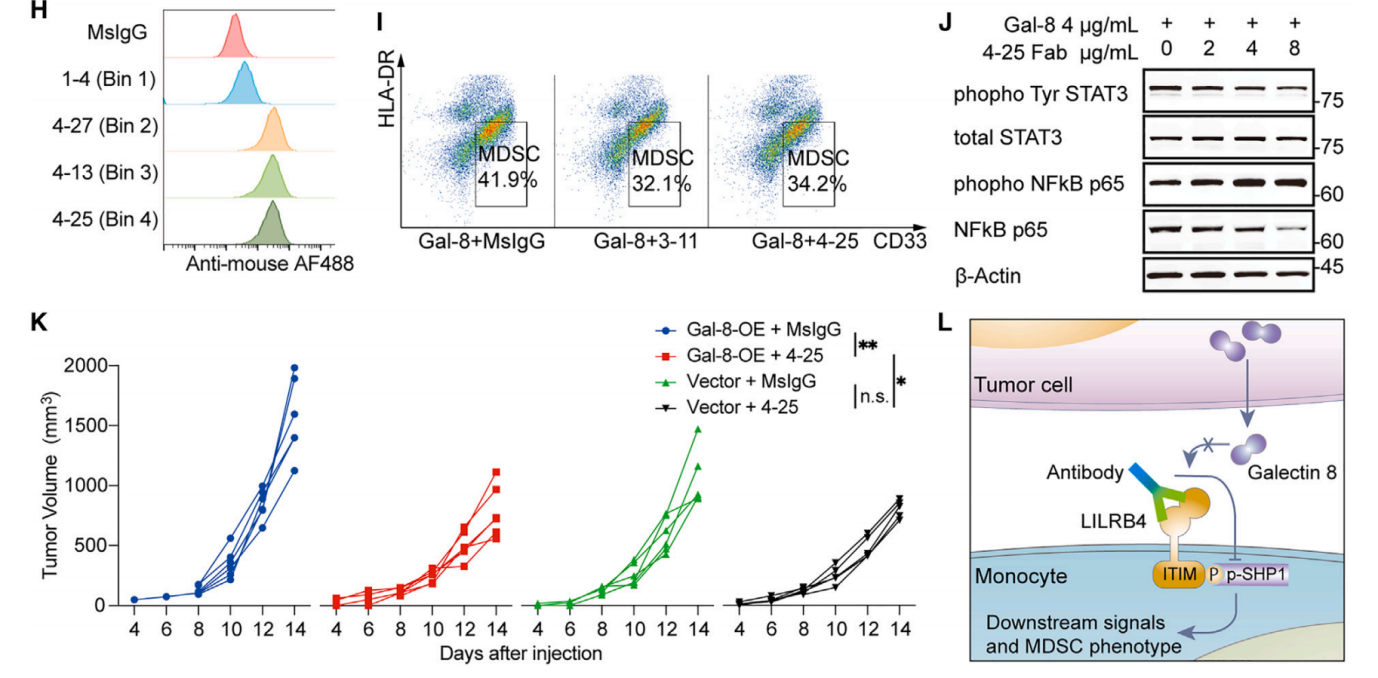
这一研究发现了LILRB4的新功能性配体Galectin-8,揭示了配体受体互作在M-MDSC诱导和肿瘤免疫抑制微环境塑造中的重要作用;探究了参与M-MDSC诱导的下游信号通路。同时,本研究开发了具有阻断功能的治疗性抗体,显示了功能性配体的发现为抗体药物的早起筛选开发提供重要依据,并提供Galectin-8的表达水平作为抗体治疗的筛选标准,具有潜在转化价值。
复旦大学生物医学研究院研究员许杰为本论文通讯作者,博士生王一婷为论文的第一作者,合作方包括上海柏全生物科技有限公司等。
论文链接:https://www.cell.com/cell-reports-medicine/fulltext/S2666-3791(23)00603-1





