先天性心脏病是新生儿最常见的出生缺陷,发病率高达0.4%~1%,也是婴幼儿死亡的主要原因之一。心脏发育受到很多基因的逐级精密调控,这些基因的突变与先天性心脏病的发生密切相关。
转录因子MESP1在发育早期瞬时表达,调控心脏前体细胞(cardiac progenitor)等的产生,但其激活早期心脏发育基因的机制仍待研究。已有报道在先天性心脏病病人中,发现了MESP1多个位点的单等位基因突变(single-allele mutation),表观遗传因子PRC1(Polycomb repressive complex 1)复合体、黏连蛋白(cohesin)复合体的多个组分也报道存在先天性心脏病致病突变,而这些组分在心脏发育中的具体作用机制还不清楚。

2022年11月21日,复旦大学基础医学院孙宁实验室和复旦大学生物医学研究院(IBS)蓝斐实验室在《发育细胞》(Developmental Cell)在线发表论文Essential role of MESP1-RING1A complex in cardiac differentiation,发现转录因子MESP1结合表观因子RING1A在心脏发育中共同发挥重要作用。
本研究首次发现MESP1可与PRC1核心蛋白RING1A相互作用,协同结合并激活人类心脏早期发育相关基因表达,如中胚层形成相关基因WNT5A、NCAM1、LEF1、ZEB2、MEIS1、MEIS2、PDGFRA、GATA6,与心脏谱系基因MYOCD和MEF2C;并发现RING1A在人类心肌细胞体外分化和小鼠心脏发育过程中发挥重要作用:RING1A缺失会导致人类心肌体外分化效率、收缩蛋白表达、钙处理能力等的下降;Ring1A敲除小鼠此前只报道过中轴骨发育异常,本研究发现Ring1A敲除小鼠出现与MESP1突变病人类似的先天性心脏病表型,如主动脉骑跨、室间隔缺损、肺动脉狭窄、致密化心室壁变薄等。
PRC1复合体的经典作用是抑制基因表达;近年来也有报道在皮肤、神经发育等过程中,PRC1可参与基因表达的激活。本研究发现MESP1-RING1A可与cohesin复合体、p300结合,通过调控A/B区室(compartment A/B)转换、增强子-启动子的染色质相互作用(chromatin interaction)、组蛋白乙酰化,激活心脏发育相关基因的表达。
本研究同时发现,MESP1致病突变会影响MESP1与RING1A、cohesin组分的结合,影响心脏发育基因的表达及心肌的正常分化。
总之,这些研究不仅证明了MESP1-RING1A在心脏发育中的重要性,同时也为MESP1,PRC1 和 cohesin组分突变导致先天性心脏病的机制提供了可能的解释。
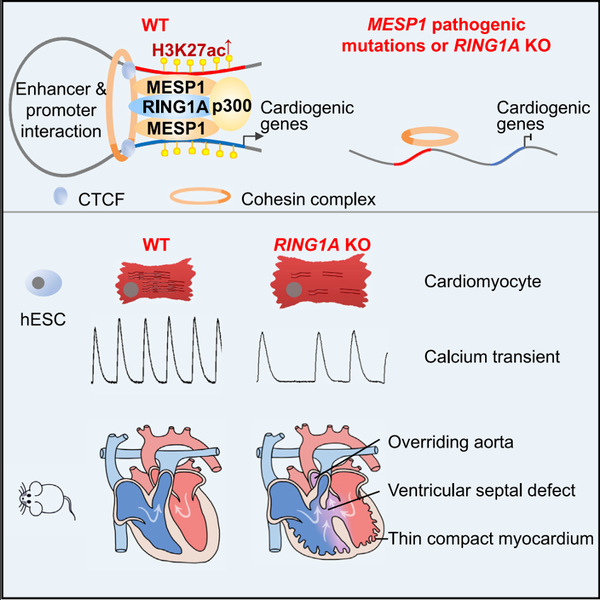
转录因子MESP1与表观遗传因子RING1A协同调控早期心脏发育
孙宁教授和蓝斐研究员为论文共同通讯作者。复旦大学基础医学院梁倩倩青年副研究员、生物医学研究院王司清博士和基础医学院博士生周心妍为共同第一作者。研究还得到了广东省人民医院的朱平教授、纪念斯隆-凯特琳癌症中心的徐一驰博士等合作者的大力支持。
原文链接:https://www.cell.com/developmental-cell/fulltext/S1534-5807(22)00761-4





