近日,复旦大学附属中山医院心内科葛均波院士、黄浙勇副教授与复旦大学药学院庞志清副研究员合作开发了一种单核工程化修饰的间充质干细胞外囊泡,用于增强干细胞外囊泡对缺血性损伤心肌的归巢和修复作用。相关成果论文以《单核细胞仿生物修饰间充质干细胞外囊泡改善其对小鼠心肌缺血再灌注损伤的归巢》(“Monocyte mimics improve mesenchymal stem cell-derived extracellular vesicle homing in a mouse MI/RI model”) 为题,在线发表于生物材料与组织工程领域国际著名期刊《生物材料》(Biomaterials)。

该文章报道了一种全新的工程化改造修饰细胞外囊泡及其靶向递送的策略。通过生物膜融合的工程化改造手段,单核细胞的仿生物赋予了干细胞外囊泡对损伤心脏显著增强的靶向趋化能力,为解决胞外囊泡产量低、归巢少、功效不确切等问题提供了新方法。
缺血性心脏病常导致大量的心肌细胞损伤和丢失。为了修复和重建心脏结构功能,以干细胞为基础的相关疗法已被广泛用于心脏修复的基础和临床研究。大量研究已经证实干细胞疗法的获益来源于其分泌的保护性物质,包括胞外囊泡。但这些细胞外囊泡存在着体内半衰期短、缺乏靶向性、脱靶效应及低产量等问题,使得临床前研究结果不尽如人意,也极大了地限制了临床转化的可能性。因此,寻求新的手段和技术克服上述问题,以增强干细胞外囊泡治疗心脏等器官缺血性损伤的疗效,具有重要的理论和实践意义。
在这项研究中,研究人员受心肌缺血再灌注损伤后单核-巨噬细胞系统对损伤区的趋化浸润特性的启发,开发了一种工程化仿生修饰的新手段。研究人员将提取的单核细胞膜囊泡作为单核细胞仿生物,通过膜融合的工程技术,将其与间充质干细胞外囊泡融合从而达到仿生修饰的目的,最终得到了具有单核细胞靶向趋化能力的干细胞外囊泡。重要的是,经工程化改造后,这种杂合干细胞外囊泡的生物学功能并无明显改变,依然保持了显著的心肌保护、促血管化和免疫调节等功效。同时,研究团队采用多模态成像技术证实,工程化胞外囊泡静脉注射后,能够靶向趋化并聚集于心肌损伤区域,这对以干细胞为基础的生物制剂的有效性和安全性是至关重要的。
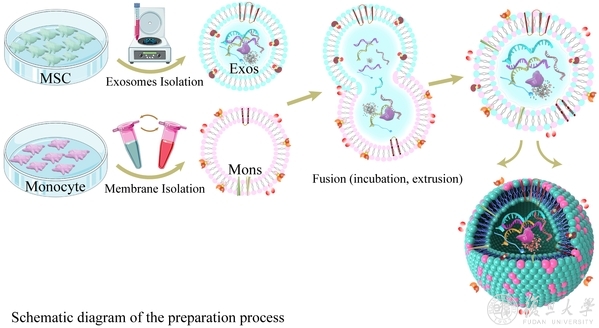
图为单核细胞仿生物修饰间充质干细胞外囊泡的构建
该项研究表明,通过工程化改造的技术,利用仿生化修饰的策略,干细胞来源的治疗性胞外囊泡可被改造,并被赋予对特定疾病的器官组织靶向归巢能力,有可能成为推动干细胞外囊泡治疗缺血性损伤所致的心血管等疾病的有力推手,因此这项研究所开发的技术手段对于脏器损伤的修复和再生医学领域的相关研究具有重要的实践意义。
复旦大学附属中山医院心内科博士生张宁和宋亚楠主治医师为该论文的共同第一作者,复旦大学附属中山医院心内科葛均波院士、黄浙勇副教授和复旦大学药学院庞志清副研究员为该论文的共同通讯作者,复旦大学为唯一作者单位。此项研究得到了来自国家自然科学基金重大研究计划项目、面上项目的支持。





