近日,美国心脏协会(AHA)官方期刊循环(Circulation,IF=14.9)杂志社对我校基础医学院生物化学系丁忠仁研究员进行了专访,并将访谈内容刊登在循环杂志社官方主页及官方社交媒体。专访中,丁忠仁研究员向国际同行介绍了复旦大学基础医学院生物化学系在循环系统模式识别受体领域的重要研究进展。
细菌病原体的急性感染后,可以发生菌血症,造成机体循环系统高凝状态,直至发生弥漫性血管内凝血(DIC),导致临床致死性严重后果。而细菌病原体的慢性感染,可以引起机体循环系统的长期高炎症负荷,从而在炎症性相关疾病如动脉粥样硬化、细菌性心内膜炎、免疫性关节炎等的发病过程中起关键作用,对人体健康造成严重危害。循环系统如何识别细菌病原体,产生高凝状态和高炎症负荷导致严重疾病?对这个问题的解答将有助于寻找合适的干预靶点和针对性的治疗策略。丁忠仁研究员和生化系张思副教授,经过5年的长期努力,对循环系统中最小的血细胞—“血小板”在识别细菌病原体的功能进行了研究,发现血小板表达有细胞内模式识别受体NOD2,血小板NOD2特异性识别革兰氏阳性菌和阴性菌的细菌骨架中,具有免疫活性的最小结构单位—“胞壁酰二肽”,在感染过程中激活丝裂原活化蛋白激酶(MAPK)途径和一氧化碳(NO)信号,增强血小板活化能力,导致循环系统高凝状态。此外,血小板NOD2通过识别胞壁酰二肽,在感染过程中激活蛋白水解酶Caspase-1,剪切IL-1β前体转化为成熟的IL-1β,导致炎症因子的大量释放,产生机体高炎症负荷。相关研究成果以论著的形式发表在心血管顶级期刊Circulation杂志。Circulation杂志对该项研究成果表现出高度重视,将其列为当期编辑推荐文章,并邀请国际著名免疫病学家哈佛大学医学院BID医学中心风湿科主任George C. Tsokos教授为文章撰写了同期评述。Tsoko教授结合实际临床问题,对丁忠仁教授的研究成果的临床应用价值进行了评述,认为该成果解释了血小板在免疫和感染性疾病发病病理的重要作用,以感染相关的自身免疫性疾病为例:在疾病发生过程中,“补体系统”担当火炬手的角色,而“血小板”则负责运送燃料,加剧疾病的进展;对NOD2受体的靶向阻断将具有治疗前景。Tsoko教授给予该成果高度评价,认为该成果和同期Circulation杂志发表的Atkinson博士的工作,共同回答了当下医学临床工作的两个重要问题—“The two accompanying papers address two important points in the current practice of medicine”。
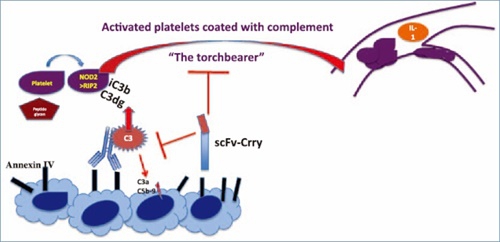
补体系统和血小板共同参与免疫性疾病进展过程
丁忠仁课题组长期从事血小板激活机制、抗血小板药作用机理和抗血小板药的新药研发工作,自2008年5月份课题组成立以来,已有多篇文章在Circulation、J Thromb Haemost、Thromb Haemost上发表,指导的研究生有多人次获得“国际血栓与止血学会(ISTH)”“Young Investigator Award”和国家奖学金, 此次Circulation文章的第一作者张思副教授2012年从丁老师课题组博士毕业。该工作受到“国家自然科学基金”和“上海高校特聘教授(东方学者)”人才基金的资助。





