非编码调控元件(cis-regulatory element)和功能性遗传变异对于人脑发育及其健康维持至关重要。人类基因组中已经发现了超过百万个非编码调控元件,包括增强子(enhancer)、启动子(promoter)等。增强子与启动子之间会形成复杂的互作网络(enhancer-promoter interaction,EPI),对于细胞组织特异性的基因表达具有重要的调控作用,并且与特定的疾病表型密切相关。
2023年7月24日,复旦大学类脑智能科学与技术研究院赵兴明教授团队在Genome Medicine上发表题为Prioritizing genes associated with brain disorders by leveraging enhancer-promoter interactions in diverse neural cells and tissues(利用多种神经细胞和组织中的增强子-启动子相互作用定位脑疾病相关的基因)的研究论文。
该研究基于FANTOM5计划(FANTOM计划的第五阶段)的439种不同的人类细胞/组织类型的RNA表达活性数据,基于机器学习方法对每一种细胞/组织类型中的EPI网络进行了重构,并利用其他来源的功能基因组学数据系统评估了重构出的EPI网络的可靠性。研究发现,重构的EPI网络显示出极强的细胞/组织类型特异性的聚集,并且与神经细胞/组织中活跃的非编码调控元件相结合的转录因子(TF)在突触可塑性和神经发育中起关键作用,如EGR1和SOX家族。
研究人员评估了17种不同的神经疾病(neurological disorder)、精神疾病(psychiatric disorder)和行为认知表型(behavioral-cognitive trait)在每一种神经细胞和脑区中活跃的非编码调控元件中的遗传力(genetic heratability)富集程度。研究发现,神经疾病大多在神经干细胞和星形胶质细胞中具有显著的遗传力富集, 而精神疾病和行为认知表型则在神经元中具有遗传力富集,此外还发现精神疾病在发育早期的大脑中具有更强的遗传力富集,暗示了不同的脑疾病类型可能具有不同的细胞和发育基础。
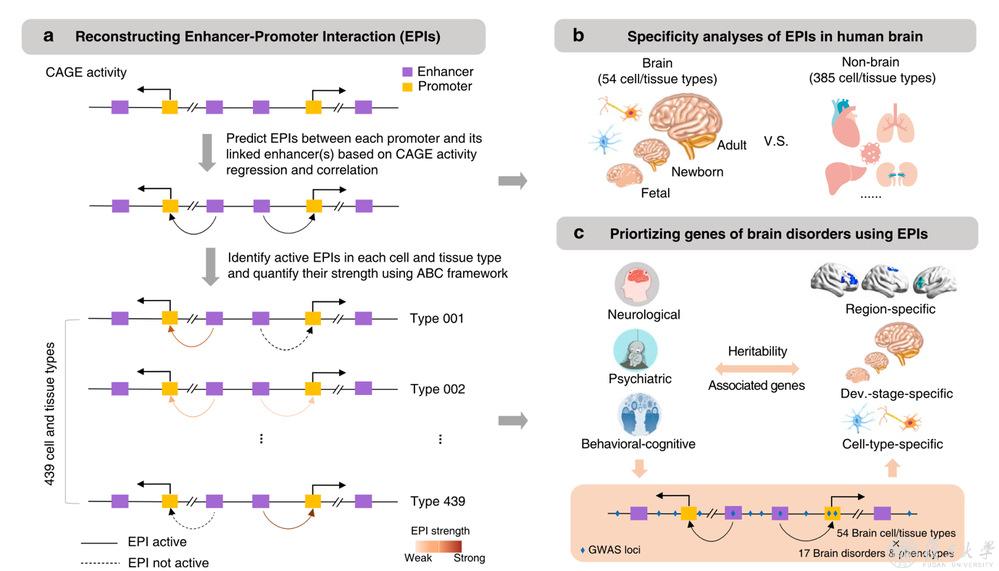
进一步,研究人员利用重构的EPI网络对脑疾病的风险基因进行了精准预测。在机制上,增强子往往调控远端的特定启动子,因此,位于增强子内部的潜在功能性遗传变异可以通过EPI网络与其特定的靶基因进行关联。基于这种假设,研究人员整合脑疾病的GWAS数据,对脑疾病相关的基因进行了系统预测。研究发现,通过EPI网络识别出的脑疾病相关基因与已知的脑疾病风险基因具有很高的重合度。进一步的分析发现,识别出的脑疾病相关基因在精神疾病和行为认知表型之间表现出广泛的基因多效性(genetic pleiotropy),同时富集与突触功能和神经系统发育相关的功能,并且与神经疾病相关基因体现出很大的差异。
综上所述,本研究构建了人脑中的非编码调控元件互作网络的概览图,分析了其在神经细胞和组织中的特异性,并据此对脑疾病基因进行了系统而精准的定位。本研究为理解脑疾病和行为认知表型的遗传调控机制提供了新见解。
复旦大学类脑智能科学与技术研究院博士生赵兴忠和宋利婷博士为论文的共同第一作者,赵兴明教授和杨禹丞青年副研究员为本文的通讯作者。本课题受到国家重点研发计划、国家自然科学基金、上海市市级科技重大专项等经费资助。
原文链接:https://genomemedicine.biomedcentral.com/articles/10.1186/s13073-023-01210-6





