近15年来,作为构建DNA纳米组装体的主要方法之一,DNA折纸术(DNA origami)可使得一条长单链DNA在成百上千条短链DNA的辅助下, 通过碱基互补配对原则折叠并锁定生成所设计的纳米图案,它的出现极大地推动了DNA纳米技术领域的发展。单链DNA折纸术(single-stranded DNA origami)是传统DNA折纸术的一种进化和衍生,它摒除了对众多短序列的需求,通过高度集成序列信息于一条长单链DNA中, 实现了单个DNA序列的自我折叠和组装体构建(类似于蛋白质由一条长肽链折叠成三维结构)。
单链 DNA组装体(ssDNs)的可编程性和可寻址性均能与传统的多链 DNA 组装体相媲美,此外它们还具有产物单一、纯净度高的先天优势及可在生物体内复制的潜力。然而,目前对于200个碱基以上的DNA序列,化学合成的成本高、产量低,当序列中包含较多的二级结构时会进一步阻碍合成的效率,这些因素限制了单链 DNA组装体在生命和材料科学等领域的应用和发展。
3月30日,复旦大学生物医学研究院顾宏周(复旦大学附属口腔医院兼职研究员)课题组在Chem杂志上发表题为“DNA-catalyzed efficient production of single-stranded DNA nanostructures”的工作,报道了一种高效制备单链DNA纳米结构的生物方法。作者通过将多个单链DNA组装体序列以假基因片段形式与自切割型DNA核酶序列有机串联成一个整体,并重组到噬菌体基因组中,实现了依托噬菌体存储组装体序列信息,可随时扩增放大并根据需求制备相应单链DNA组装体的策略。

作者以一条由520个碱基的序列折叠而成的三角形组装体为例,展示了制备方法的整个流程(图1)。首先,通过电脑程序辅助设计出可自组装成三角形的长单链DNA序列;
随后,把该组装体序列作为一个假基因片段进行化学合成,并在片段的两端各自插入一个Zn2+依赖的自切割型DNA核酶(有催化能力的核酸序列);接着,将该片段重组到质粒或噬菌粒中,通过体外或体内的滚环复制扩增方式放大制备单链DNA序列;最后,在添加Zn2+的条件下,DNA核酶自发切割并释放出单链DNA组装体序列。
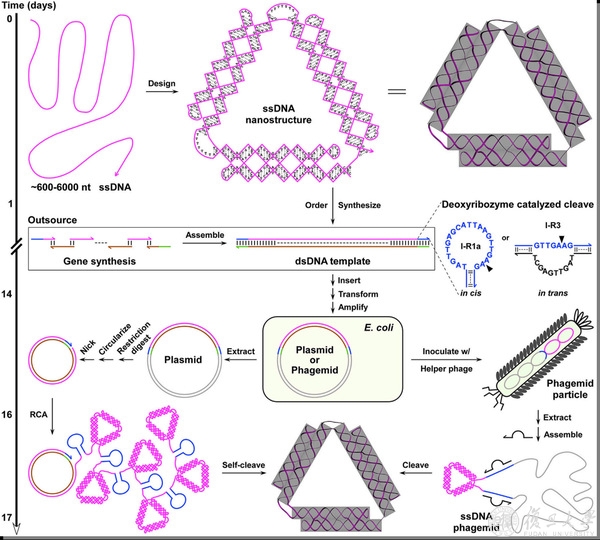
图1 利用自切割型DNA核酶制备单链DNA组装体的示意图和时间表
此外,在前人利用顺式(cis)DNA核酶制备单链DNA的基础上,作者拓展了活性更强的反式(trans)核酶的使用。当多种不同形状(三角形,520 nt;四边形,680 nt;菱形,2200 nt;方形结,1700 nt)的单链DNA组装体出现时有所需的状况时(图2),作者提出以串联多个组装体和反式核酶序列的方式,既能在重组和放大过程中节约时间和劳动力,又能在切割分离目的组装体时获得高效性和可控性。依托基于反式核酶的生物法,作者制备单链DNA组装体时成本可低至1500 rmb/g,产量可达g-kg,长度可至10000个碱基以上。
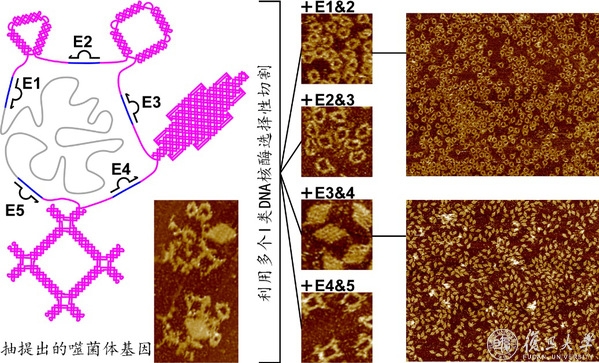
图2 利用反式(trans)切割型DNA核酶高效可控地分离制备单链DNA组装体
综上,该研究提出了一种利用反式切割型DNA核酶突破化学合成长单链DNA序列瓶颈的生物法策略,为单链DNA组装体的高效制备奠定了基础,也为基于DNA组装体的下游应用,如辅助脂质体分离制备及研究细胞对脂质体的摄取等扫清了障碍。此外,长单链DNA序列的高效制备还可能为基于长程单链DNA片段的基因敲入、基于长程锁式探针的长程测序等新技术的发展提供支撑。
在同一时期内,复旦大学生物医学研究院顾宏周研究组与耶鲁大学林晨翔研究组合作在Nature Chemistry期刊上发表题为“Sorting sub-150-nm liposomes of distinct sizes by DNA-brick-assisted centrifugation”的文章,报道了一种全新的利用DNA纳米组装体辅助脂质体按粒径大小精确分选的策略。作者在本研究中同步开发的高效制备单链DNA组装体的新方法也为大规模辅助分选脂质体提供了原材料的保障。
脂质体是临床应用最为广泛的纳米药物载体之一,其粒径大小和表面修饰等性质是影响递药效率的关键因素。此前,由于制备的脂质体的粒径区分度和均一性都较差,对于粒径影响细胞摄取脂质体的分析研究多停留在较为模糊的定性层面,从而导致了药物制备工艺中对脂质体粒径大小的规定缺乏精细的定量标准。
作者在解决了单链DNA组装体在辅助分离脂质体时作为一种消耗型材料的来源和成本问题后,大量(mg-g级)地制备了在40-100 nm范围内的粒径精确均一的包裹了DNA组装体的脂质体;随后,作者选取40, 72和96 nm的三种粒径大小的脂质体和多种细胞孵育,研究粒径对细胞摄取脂质体的影响,研究结果表明,与正常的HEK293T细胞相比,肿瘤细胞(HeLa细胞和MDA-MB-231细胞)更容易吞噬这些包裹了DNA组装体的脂质体,且摄取量最多的粒径为96 nm;此外,当脂质体表面的DNA组装体被去除后,所有细胞摄取脂质体的效率都显著降低。这些现象表明脂质体的粒径大小和表面修饰的DNA组装体共同影响着细胞对脂质体的摄取。
下一步,作者计划将DNA组装体辅助制备的脂质体的粒径范围扩大至150 nm,系统地测量和分析各种肿瘤细胞对脂质体摄取的最佳粒径区间、各种正常细胞对脂质体低效摄取粒径区间,以及脂质体靶向各类组织和器官的最佳粒径区间等,以期为设计更安全高效的脂质体药物载体平台提供有力的数据。
据悉,第一篇发表在Chem的论文中,复旦大学生物医学研究院及复旦大学附属口腔医院顾宏周研究员为本文通讯作者,贾友礼(复旦大学)、陈黎曼(复旦大学/附属肿瘤医院)为本文的共同第一作者;在另一篇Nature Chemistry的论文中,耶鲁大学医学院林晨翔教授和复旦大学生物医学研究院顾宏周研究员为本文的共同通讯作者,杨洋(耶鲁大学/上海交通大学)、吴振永(耶鲁大学)为本文共同第一作者,夏凯(复旦大学/附属中山医院)为本文的数据重复等提供了重要的支持。
论文链接:
1、https://www.cell.com/chem/fulltext/S2451-9294(20)30633-1
2、https://www.nature.com/articles/s41557-021-00667-5





