细胞的命运决定受到转录因子与表观遗传因子的协同调控,例如胚胎干细胞的多能性维持,既需要关键转录因子的正确结合,又需要对启动子和增强子活性的精确调控,两者密不可分。因此,研究转录因子与表观遗传因子如何协同作用维持干细胞多能性是亟需解决的科学问题,对细胞命运决定具有重要的意义。近日,复旦大学基础医学院教授孟丹团队与生物医学研究院研究员蓝斐团队合作揭示了转录因子与表观遗传因子协同调控干细胞命运决定的新机制。1月27日,研究成果以《BACH1招募NANOG和组蛋白H3赖氨酸4甲基转移酶MLL/SET1复合物调节增强子-启动子活性并维持干细胞多能性》(“BACH1 recruits NANOG and histone H3 lysine 4 methyltransferase MLL/SET1 complexes to regulate enhancer–promoter activity and maintains pluripotency”)为题在线发表于《核酸研究》(Nucleic Acids Research)。该研究揭示了转录因子BACH1(BTB and CNC homology 1)在维持小鼠胚胎干细胞多能性和决定干细胞命运中发挥的关键作用及作用机制,对于干细胞命运调控的研究具有重要的科学意义。

研究团队前期在《科学进展》(Science Advances)上发表的研究中,发现BACH1是干细胞维持自我更新和决定谱系分化的关键调控因子。但是BACH1是否参与调控染色质修饰进而维持干细胞多能性还不清楚。研究发现BACH1可以分别直接结合转录因子NANOG和表观遗传因子H3K4甲基化酶MLL/SET1复合物,共同招募它们到染色质上(尤其是染色质环的锚点处),调控基因启动子和增强子的H3K4me3水平,调控下游基因(尤其是多能性基因)的转录活性,进而维持小鼠胚胎干细胞多能性。干细胞中NANOG和H3K4甲基化酶MLL/SET1复合物可以相互作用,但敲除BACH1基因会显著破坏这种相互作用,并且降低它们在染色质上的结合,降低H3K4me3水平,降低增强子活性与下游基因转录活性。这提示BACH1像桥梁一样,沟通了NANOG和MLL/SET1复合物,共同调控启动子-增强子活性。BACH1结合了小鼠胚胎干细胞中约70%的超级增强子,这些超级增强子上有H3K4me1和H3K4me3共存。而敲除BACH1基因后,则会发生H3K4me3下降和H3K4me1的上升,同时伴随着MLL/SET1复合物的结合强度下降。这提示H3K4me1和H3K4me3的转换,可能是由于同一种甲基化酶的催化活性/催化时间发生了变化导致的。此外,研究人员也发现BACH1可以调控糖酵解和氧化磷酸化的很多基因,而代谢类型的转换也被认为是干细胞命运决定的一个重要调控方式。
这项研究揭示了BACH1与转录因子NANOG和表观遗传因子MLL/SET1复合物协同作用,调控启动子-增强子环的组蛋白修饰与活性,进而维持胚胎干细胞多能性。研究结果阐明了干细胞全能性调控的新机制。
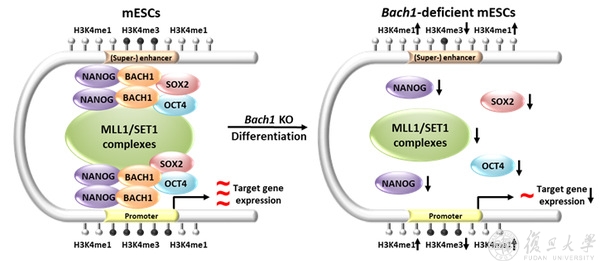
BACH1招募NANOG和H3K4甲基化酶MLL/SET1复合物调节增强子-启动子活性并维持干细胞多能性的示意图
复旦大学的牛琮、王司清、郭阶雨、魏香香、贾孟萍是论文的共同第一作者,复旦大学教授孟丹和研究员蓝斐是共同通讯作者,复旦大学为第一作者单位。这项研究得到了中科院马普研究所/北京大学教授韩敬东及博士生陈钊熊和龚文轩的大力支持。
论文链接:https://doi.org/10.1093/nar/gkab034





