人体免疫反应包括固有免疫和适应性免疫。当病原体入侵宿主后,首先启动固有性免疫反应,其中抗病毒免疫中主要发挥作用的是Ⅰ型干扰素及其调控的信号通路。IFNβ可以激活JAK-STAT通路,促进TNFα、IL-6等大量炎症因子的表达,从而启动机体抗病毒免疫反应。
近日,《自然-通讯》(Nature communications)在线发表了复旦大学基础医学院免疫学系严大鹏团队题为“β-arrestin 2 as an activator of cGAS-STING signaling and target of viral immune evasion”研究论文。该研究揭示了β-arrestin 2通过cGAS调节Ⅰ型干扰素通路的分子机制,而病毒通过降解β-arrestin 2实现其免疫逃逸的目的。
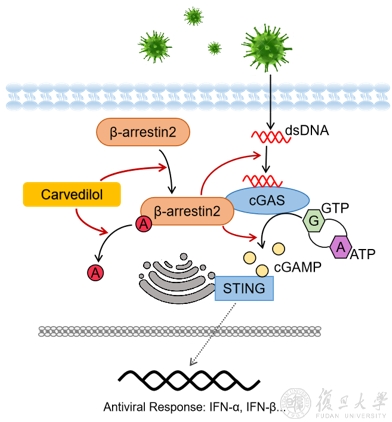
严大鹏课题组发现β-arrestin 2促进IFNβ的表达、Ⅰ型干扰素信号通路的活化及小鼠的抗病毒免疫。机制上,β-arrestin 2与cGAS直接结合并促进cGAS和DNA的结合及cGAMP的产生,而β-arrestin 2在感染中发生的去乙酰化是其发挥抗感染功能的基础。在病毒感染早期,β-arrestin 2迅速发生去乙酰化而活化,发挥其抗感染功能;而在感染晚期,β-arrestin 2却能被病毒诱导,发生泛素化而被降解,帮助病毒实现免疫逃逸。然而,“魔高一尺,道高一丈”。团队进一步研究发现,抗心衰药物Carvedilol能够促进β-arrestin 2的去乙酰化及抑制β-arrestin 2的降解,通过稳定β-arrestin 2调控Ⅰ型干扰素信号通路及小鼠的抗病毒免疫,提示其可作为潜在的抗病毒药物。
复旦大学基础医学院免疫学系2017级直博生张懿华和2019博士生李慢慢为本文的共同第一作者,严大鹏为本文的通讯作者。





