肿瘤免疫治疗药物,未来可能可以口服了?复旦大学的最新研究成果,为此提供了潜在的技术基础。
北京时间2026年3月19日晚,复旦大学鲁伯埙与粤港澳大湾区精准医学研究院宋海坤团队联合海军军医大学盛春泉团队,在《细胞》(Cell)杂志在线发表题为“Hijacking ER-associated degradation (ERAD) for targeted degradation of transmembrane proteins”的研究论文。
研究团队巧妙利用跨膜蛋白质大部分需进入内质网折叠的特性,驾驭细胞自身的内质网相关降解机制(ER-associated degradation,ERAD),开创性地建立了一种全新的靶向蛋白降解策略,并命名为ERAD-engaging chimera(ERADEC)。
该研究突破了现有主流靶向降解技术的部分局限,利用小分子化合物实现了对跨膜蛋白的高效、选择性降解,未来有望推动肿瘤免疫治疗进入“口服时代”,并为其他多种由膜蛋白引起的疾病提供药物研发全新技术路径。
精准“劫持”细胞工厂,清理致病蛋白
如果将细胞比作一座精密运行的工厂,那么蛋白质就是这座工厂里最核心的“产品”。在细胞内部,每天都有海量的蛋白质被合成、折叠、运输与降解,任何一个环节出错都可能产生“次品蛋白”,进而导致疾病。
为保证“生产质量”,细胞进化出了一套精密的“质量控制系统”。其中,内质网犹如质检和初包装车间,内质网相关降解通路(ER-associated degradation,ERAD)负责识别那些由于折叠异常或质量不合格的送往内质网的蛋白,利用内质网上一类特殊的功能性蛋白(E3泛素化连接酶)打上“垃圾”(泛素化)的标签,进一步通过反向移位、去泛素化、重新泛素等一系列复杂生化反应,最终送入“垃圾处理站”(蛋白酶体)进行清除。
长期以来,这套系统被认为主要承担清理“残次品”的任务。然而,复旦大学研究团队提出了一个大胆的设想:能否人为地利用小分子化合物将某些致病蛋白引入这一通路,利用细胞自身的质量控制机制,实现对特定蛋白的精准降解?这一大胆设想,带来了靶向蛋白降解领域的重要突破。
蛋白靶向降解技术,即设计并利用化合物选择性清除特定靶蛋白的前沿技术,可从根本上消除致病蛋白的病理功能,为阐明疾病的机制以及探寻新的干预策略提供重要工具乃至治疗药物。此类技术为生物医药发展提供了革命性进展,也是目前小分子药物领域最具前景的方向之一。
然而,现有主流降解技术PROTAC(Proteolysis-Targeting Chimera,蛋白降解靶向嵌合体)等,虽能高效降解许多胞质或核内蛋白,但对大多数跨膜蛋白的作用十分有限。其关键原因在于,部分要贴在细胞工厂外墙上的产品(膜蛋白)或要运出工厂的产品(分泌蛋白),它们的生产流程很特殊,在生产线上刚造出雏形,就会立刻被送进内质网进行折叠,并被装车(囊泡)转运出去,难以被依赖于细胞浆环境的传统降解机制捕捉。
尽管科学界近年来开发了一系列新技术,如LYTAC、GlueTAC、PROTAB、IFLD、TransTAC、SPTAC等尝试解决这一问题,但它们大多依赖于修饰的生物大分子,不具备小分子化合物可口服、免疫原性低、价格低廉等优势。此外,这些技术基本都依赖于内体-溶酶体途径(endosome-lysosome),因而对跨膜蛋白的降解效率大大受到循环内体(recycling endosomes)的影响,且依赖于特定的细胞膜受体。
能否开发独立于内体-溶酶体途径的跨膜蛋白靶向降解技术呢?面对这一挑战,复旦大学生命科学学院教授鲁伯埙团队将目光投向了尚未被开发利用的细胞内蛋白降解通路——内质网相关降解(ERAD)途径。他们的核心思路是:设计一种小分子化合物作为“桥梁”,一端钩住内质网上的关键酶,另一端识别并抓住致病的跨膜蛋白,从而“劫持”内质网自身的降解系统,在“质检车间”内就将目标蛋白销毁。

鲁伯埙团队合影
“这个方法之前还没有人尝试过,一方面找到能精准结合内质网关键酶的小分子很难;另一方面,学界传统认为ERAD系统主要负责降解错误折叠蛋白,是否能驾驭它去降解折叠完成且功能正常的蛋白尚需探索。”鲁伯埙解释。
一把钥匙开多把锁:开辟跨膜蛋白靶向降解新平台
研究的关键,在于能否找到可以“劫持”内质网降解系统的小分子,进而将目标蛋白“送进”内质网膜,通过内质网系统进行降解。
机缘巧合,团队的确找到了这样的小分子化合物——他们在前期针对亨廷顿病的致病蛋白mHTT的降解研究中发现,小分子化合物desonide能够与内质网E3泛素连接酶SYVN1直接结合,促进其泛素化mHTT,进而诱导其降解。
基于此,他们提出了ERADEC(ERAD-engaging chimera)的原创构想:以desonide作为结合SYVN1的接头化合物,连接针对不同靶蛋白的配体,其结构类似于一座桥梁:一端结合SYVN1,另一端识别目标蛋白,中间通过化学连接子相连。当ERADEC同时结合这两个分子时,就会形成稳定的三元复合物,进而触发目标蛋白的泛素化和降解。
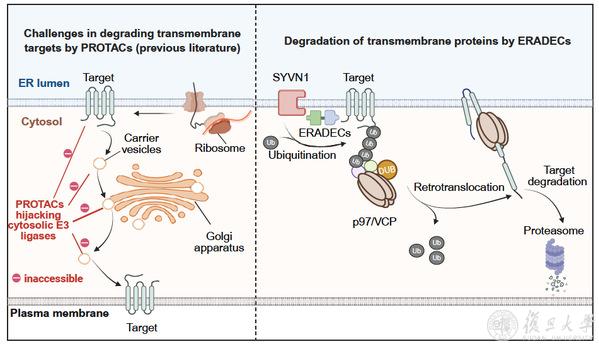
传统PROTACs与新型ERADECs的降解机制对比
研究人员首先以肿瘤免疫治疗的关键靶点PD-L1蛋白为模型进行验证。实验结果显示,ERADEC能够显著降低细胞内PD-L1的蛋白水平,并且这一过程严格依赖于SYVN1及ERAD通路。在人免疫细胞重构的小鼠肿瘤模型中,ERADEC表现出显著的抗肿瘤效果,甚至优于临床上已广泛应用的PD-L1抗体药物。
更重要的是,ERADEC策略展现出平台技术的潜力,为靶向蛋白降解领域推开了一扇新的大门。通过改变目标配体,研究团队成功实现了对多种不同跨膜蛋白的降解。这意味着该技术有望被拓展应用于肿瘤、代谢性疾病、神经退行性疾病等多个领域,为针对跨膜蛋白的药物开发打开了全新局面。
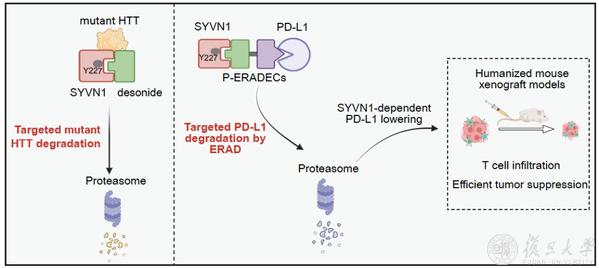
ERADECs 在特定疾病靶点上的应用实例
过去十余年,PROTAC等技术主要依赖细胞质中的E3连接酶,而ERADEC则首次系统性地利用了内质网质量控制体系。这种思路的转变,为跨膜蛋白这一长期难以干预的靶点,带来了全新的降解可能。
告别静脉注射?肿瘤免疫治疗有望迎来“口服时代”
这项突破性研究,实际上源于一个意外。团队在筛选亨廷顿病致病蛋白降解分子的过程中,发现了一个有效小分子,但起初无法解释其作用机制。2022年,这项发现发表于PNAS期刊。
“没有找到科学现象背后的机制,总觉得十分遗憾。”鲁伯埙教授没有放弃,带领团队又深入探索了一年多,最终将机制锁定在内质网E3连接酶上,从而催生了ERADEC这一全新的技术方向。
在2024年的某次学术会议上,鲁伯埙曾专门请教ERED领域的权威专家Kazutoshi Mori(拉斯克奖和科学突破奖得主),对方肯定了他的设想的原创性和可行性,鼓励他继续深耕,挖掘ERAD路径在靶向降解上的更多可能性。

鲁伯埙
值得一提的是,AI for Science的理念在这项研究中得到了充分发挥。团队借助大模型来预测蛋白的三维结构,以及小分子和蛋白的结合模式。“AI工具帮助我们理解了小分子具体结合在什么位置,这些信息对后续的分子改造至关重要。”鲁伯埙介绍。
从观察现象到大胆构想,再到成果发表,用时近十年打磨,团队成功证明了“利用内质网降解系统来靶向膜蛋白”这一全新思路的可行性,这也是国际首个基于ERAD途径开发的靶向降解技术。

宋海坤
对于未来的应用前景,鲁伯埙教授充满期待:“本文报道的小分子本身不能口服,但通过新的筛选和药物化学改造,我们已获得了有一定口服利用度的ERADEC分子。如果未来能开发出口服药,患者将无需频繁去医院注射,在家即可服药,这将极大地提高治疗可及性和患者生活质量。”
他进一步比较了其与传统抗体药的优势:抗体药物需要饱和结合绝大部分靶蛋白才能起效,而且几乎不可能口服,需静脉注射或更复杂的药物递送方法,价格也较昂贵。而小分子降解剂可以从根源上清除靶蛋白,所需药物浓度极低(本文所发现的PD-L1降解化合物在皮摩尔到纳摩尔量级即有效),且作用可能更彻底、成本更低、副作用更小。
“以抗肿瘤PD-L1药物为例,抗体药物需要有足够多的抗体把表面绝大多数的PD-L1都结合,才能有效阻止它的作用,抗体一旦随着代谢消除或者浓度不够高,露出一些PD-L1,癌细胞又会重新逃逸。而小分子药物的原理是降解化合物,可以彻底把细胞膜表面的PD-L1给降解掉,降解后小分子可以像催化剂一样被重复利用,因此只需要结合很小部分的PD-L1然后循环催化降解过程即可发挥作用。”他解释。
目前,论文相关专利已与相关药企签署许可协议,团队也正在加快推进第二代小分子的系列药物研发,旨在针对不同的疾病靶点,使这项基础学科科学发现真正惠及广大患者。
复旦大学为本论文第一完成单位。复旦大学鲁伯埙、海军军医大学盛春泉教授为论文通讯作者,粤港澳大湾区精准医学研究院宋海坤、海军军医大学王蔚、粤港澳大湾区精准医学研究院梅婷芳、复旦大学郑惠文为论文的共同第一作者。复旦大学教师服部素之、刘瑞、丁澦、费义艳,及上海交通大学教师曹禹等为该研究作出了重要贡献。该研究得到了国家自然科学基金、新基石研究员等项目的支持。
论文链接:https://www.cell.com/cell/abstract/S0092-8674(26)00105-4





